恒瑞創(chuàng)新藥硫酸艾瑪昔替尼片獲批類風濕關(guān)節(jié)炎新適應癥
3 月 21 日,NMPA 官網(wǎng)顯示,恒瑞 1 類新藥 JAK1 抑制劑艾瑪昔替尼(代號: SHR0302)國內(nèi)首次獲批上市,用于治療對一種或多種TNF抑制劑療效不佳或不耐受的的活動性強直性脊柱炎(AS)的成人患者(受理號:CXHS2300071)。
艾瑪昔替尼是恒瑞自主研發(fā)的高選擇性的口服 JAK1 抑制劑,可通過抑制 JAK1 信號傳導發(fā)揮抗炎和抑制免疫的生物學效應。
此次「艾瑪昔替尼」強直性脊柱炎獲批是基于一項多中心、隨機、雙盲、安慰劑對照的 II/III 期臨床研究 SHR0302-302(NCT04481139)的積極結(jié)果。恒瑞在 2024 年 EULAR 年會上公布了此項研究的結(jié)果
結(jié)果顯示,艾瑪昔替尼 4 mg 對 NSAIDs 反應不足或禁忌癥的活動性 AS 受試者的疾病活動度、體征和癥狀方面均顯示出顯著的改善。
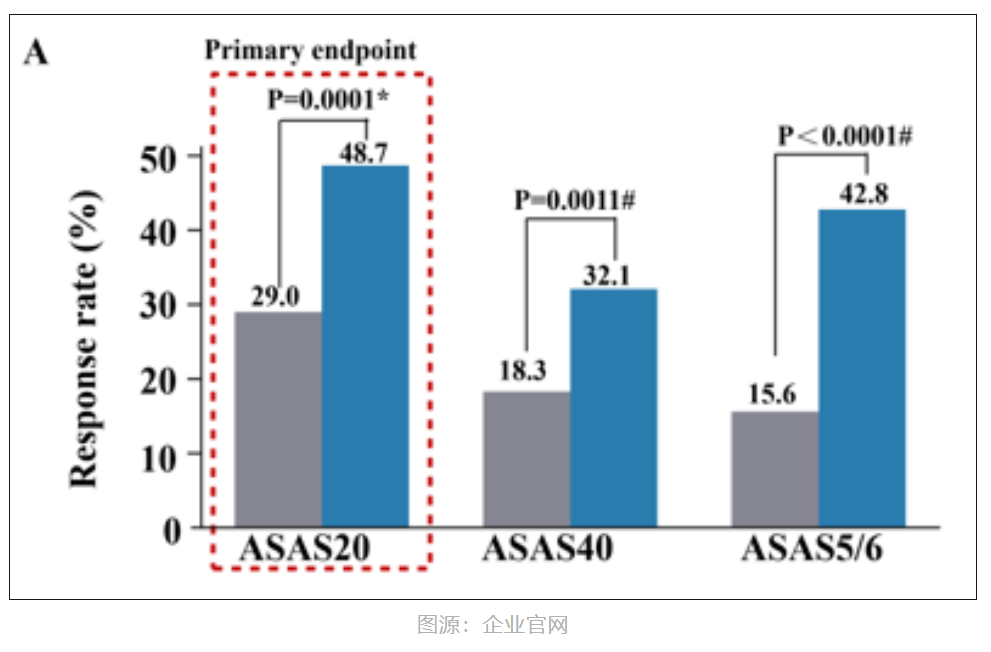
1)第 12 周時,艾瑪昔替尼 4 mg 組在 ASAS20(48.7% vs. 29.0%)、ASAS40(32.1% vs. 18.3%)和 ASAS5/6 應答(42.8% vs. 15.6%)方面存在顯著改善。
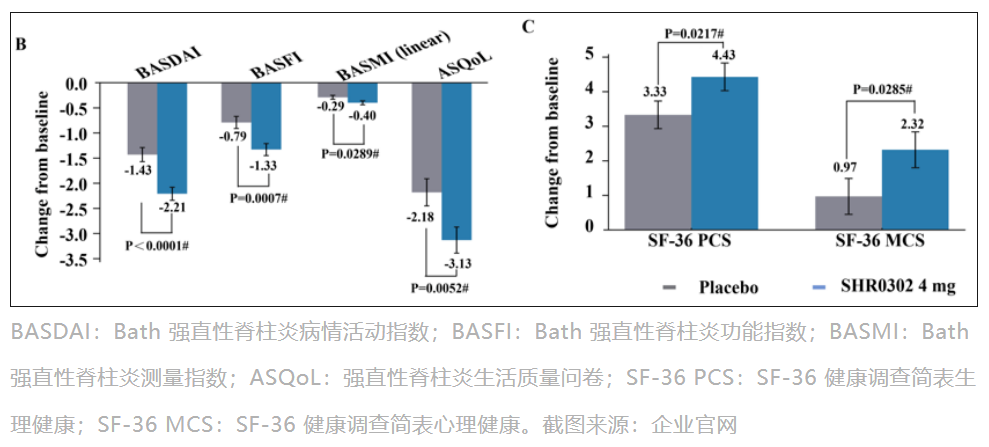
2)第 12 周時,BASDAI、BASFI、BASMI、 ASQoL、SF-36 PCS 和 SF-36 MCS 較基線變化均大于接受安慰劑治療的受試者。
3) 安全性方面,整個試驗過程中,未報告死亡、結(jié)核病病例、重大心血管事件、血栓栓塞事件或新發(fā)惡性腫瘤,也未發(fā)現(xiàn)新的安全性事件。
Insight 數(shù)據(jù)庫顯示,此前全球有 4 款 JAK1 靶點新藥已被批準上市,其中國內(nèi)已獲批 3 款,分別是輝瑞的阿布昔替尼、艾伯維的烏帕替尼和迪哲醫(yī)藥的戈利昔替尼。恒瑞的艾瑪昔替尼成為國內(nèi)第 4 款、國產(chǎn)第 2 款獲批上市的 JAK1 抑制劑。

目前這四款 JAK1 抑制劑在國內(nèi)獲批的適應癥存在差異:
輝瑞的阿布昔替尼適用于特應性皮炎;
艾伯維的烏帕替尼的適應癥廣泛,包括特應性皮炎、類風濕關(guān)節(jié)炎、銀屑病關(guān)節(jié)炎、潰瘍性結(jié)腸炎、克羅恩病、放射學陰性中軸型脊柱關(guān)節(jié)炎、強直性脊柱炎;
迪哲醫(yī)藥的戈利昔替尼適用于外周 T 細胞淋巴瘤;
恒瑞的艾瑪昔替尼適用于強直性脊柱炎。
值得注意的是,恒瑞艾瑪昔替尼還開展了包括潰瘍性結(jié)腸炎、特應性皮炎、斑禿、放射學陰性中軸型關(guān)節(jié)炎等多個適應癥的臨床研究,其中還有 3 個新適應癥(斑禿、特應性皮炎、類風濕性關(guān)節(jié)炎)已進入申請上市階段。
當然,恒瑞對于艾瑪昔替尼的布局,除了本次獲批的口服片劑,還包括了皮膚制劑和外用混懸劑。
2018 年 1 月 4 日,恒瑞和美國 Arcutis 公司就用于皮膚疾病治療的局部外用制劑艾瑪昔替尼達成協(xié)議。協(xié)議授權(quán) Arcutis 公司在美國、歐盟和日本的獨家臨床開發(fā)、注冊和市場銷售的權(quán)利。作為回報,恒瑞最多可獲得共 2.23 億美元的首付款和里程碑款,外加銷售提成。
(來源:國家藥監(jiān)局、恒瑞官網(wǎng)、Insight 數(shù)據(jù)庫)